- Почему кишечник не работает после операции
- Тонкокишечная непроходимость после операции
- Толстокишечная непроходимость после операции
- Видео техники проведения очистительной клизмы
- Запор после операции
- Причины развития запора после операции
- Симптомы запора
- Общая схема лечения послеоперационных запоров
- МИКРОЛАКС ® : помощь при запоре после операции
- Почему кишечник не работает после операции
- Актуальность проблемы
- Профилактика
Почему кишечник не работает после операции
После абдоминального или тазового хирургического вмешательства у большинства больных наблюдается кишечная непроходимость той или иной степени. Точный механизм нарушения моторики ЖКТ неизвестен, но, по-видимому, оно связано с открытием перитонеальной полости, манипуляциями с кишечным трактом и продолжительными хирургическими вмешательствами.
Инфицирование, перитонит и нарушение баланса электролитов также могут привести к кишечной непроходимости. У большинства больных, подвергающихся операциям по поводу злокачественных новообразований половых органов, степень кишечной непроходимости минимальна и функционирование ЖКТ восстанавливается относительно быстро, позволяя возобновить нормальный прием пищи через несколько дней после операции. Больные с длительным ослаблением перистальтики, метеоризмом, тошнотой и рвотой нуждаются в дальнейшем обследовании и более агрессивном лечении.
При кишечной непроходимости характерно вздутие. Вначале необходимо провести физикальное исследование, оценивая качество кишечных звуков, болезненные ощущения или реакцию на пальпацию живота. Возможно, симптомы могут быть связаны с более серьезной кишечной непроходимостью или другим осложнением со стороны ЖКТ.
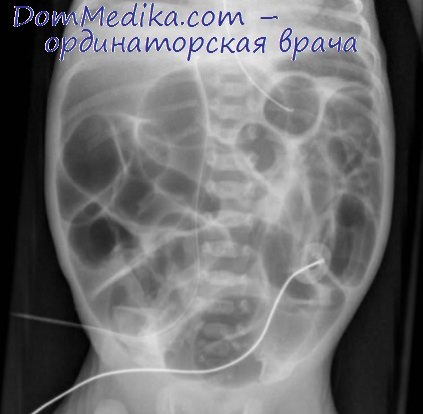
Для исключения тазового абсцесса или гематомы, которые могут поддерживать кишечную непроходимость, необходимо исследование органов таза. Проводят рентгенографию в положении пациентки лежа на спине и стоя. При этом часто определяются растянутые петли тонкой и толстой кишки с уровнями жидкости. Свободный газ в брюшной полости на рентгенограммах выявляется в течение 7—10 дней после операции и не указывает на перфорацию внутренних органов.
Для исключения дистальной обструкции толстой кишки или псевдообструкции (синдром Огилви) при расширении слепой кишки проводят ректальное исследование, ректосигмоидоскопию или ирригоскопию.
При послеоперационной кишечной непроходимости проводят декомпрессию ЖКТ и коррекцию водно-электролитных нарушений.
• Для удаления жидкости и газов из желудка устанавливают назогастральный зонд. Постоянная назогастральная аспирация желудочного содержимого позволяет эвакуировать воздух, попавший в желудок при глотательных движениях и служащий основным источником газа в тонкой кишке.
• Проводят коррекцию водно-электролитных нарушений. При кишечной непроходимости значительное количества жидкости выходит в третье пространство, т. е. скапливается в кишечнике и брюшной полости. Рвота приводит к метаболическому алкалозу и другим нарушениям баланса электролитов. Необходимы тщательный мониторинг и своевременное возмещение потерь жидкости и электролитов.
• В большинстве случаев моторика восстанавливается через несколько суток после начала лечения. Улучшение характеризуется уменьшением вздутия живота, нормализацией кишечных шумов, отхождением газов, самостоятельным стулом. Если данных физикалыюго исследования для оценки состояния больной недостаточно, повторяют рентгенографию брюшной полости.
• После нормализации функционирования ЖКТ назогастральную трубку удаляют и разрешают прием жидкой пищи.
• Если у больной не наблюдают никаких признаков улучшения в течение 48—72 ч, выясняют другие причины непроходимости. Такими причинами могут быть перитонит, нераспознанные повреждения мочеточников, ЖКТ или водно-электролитные нарушения, прежде всего гипокалиемия. При стойкой кишечной непроходимости обычно оценивают пассаж водорастворимого контраста по ЖКТ

Тонкокишечная непроходимость после операции
Тонкокишечная непроходимость после абдоминальной хирургии встречается примерно у 1—2 % больных, но может быть и чаще после радикальных операций по поводу злокачественных новообразований половых органов, вследствие обширного хирургического вмешательства или значительных манипуляций с тонкой кишкой. Чаще всего причиной тонкокишечной непроходимости бывает образование спаек на месте оперативного вмешательства.
Если тонкая кишка склеивается в перекрученном состоянии, частичная или полная непроходимость может стать следствием расширения либо отека стенки кишки. Изредка причиной тонкокишечной непроходимости могут стать ущемление тонкой кишки в грыже послеоперационного рубца, необнаруженные повреждения тонкой кишки или брыжейки толстой кишки. В начале консервативной терапии можно применять методы, характерные для лечения кишечной непроходимости.
Вследствие риска окклюзии мезентериальных сосудов и ишемии или прободения необходимо обращать пристальное внимание на усиление абдоминальной боли, прогрессирующее растяжение кишечника, лихорадку, лейкоцитоз или ацидоз, т. к. может потребоваться немедленное хирургическое вмешательство.
В большинстве случаев послеоперационная тонкокишечная непроходимость бывает лишь частичной и симптомы, как правило, устраняются консервативным лечением.
• После нескольких дней консервативного лечения может потребоваться дальнейшее обследование.
• Назначают ирригоскопию и серию исследований верхних отделов ЖКТ, включая топкую кишку. В качестве альтернативы для определения локализации непроходимости можно использовать КТ абдоминальной и тазовой полостей с гастроинтестинальным контрастом, а также провести исследование на наличие или отсутствие лимфатической кисты либо повреждения мочеточника. В большинстве случаев полной непроходимости не выявляют, хотя о локализации обструкции может свидетельствовать сужение сегмента тонкой кишки.
• Далее проводится назогастральная декомпрессия и в/в замещение жидкости, что устраняет отек стенки кишки или перекручивание брыжейки.
• При увеличении времени, необходимого для устранения осложнения, и при плохом питательном статусе больной может потребоваться ППП.
• Консервативное лечение послеоперационной тонкокишечной непроходимости, как правило, приводит к полному излечению. Однако, если признаки непроходимости сохраняются, то после полного обследования и адекватного лечения может потребоваться диагностическая лапаротомия, чтобы оценить и устранить обструкцию. В большинстве случаев необходимо разделение спаек на веем протяжении, но может потребоваться резекция тех сегментов тонкой кишки, где спаечный процесс плохо устраняется или вызывает сильное склерозирование, а также наложение анастомоза.
Толстокишечная непроходимость после операции
Чрезвычайно редко после операций по поводу злокачественных новообразований половых органов развивается толстокишечная непроходимость. К толстокишечной непроходимости у оперированных больных чаще всего приводит поздняя стадия рака яичника (РЯ); причиной непроходимости служит сдавление толстой кишки извне опухолью малого таза. Клинически недиагностированные поражения толстой кишки (например, рак) также могут привести к непроходимости. Если подозрение па непроходимость подтверждается метеоризмом, расширением толстой и слепой кишки при рентгенографии, необходимо дальнейшее исследование с помощью ирригоили колоноскопии.
Расширение слепой кишки на рентгенограмме более чем на 10 — 12 см в диаметре требует немедленной оценки и проведения декомпрессии с помощью колэктомии или колостомии. В некоторых случаях при эндоскопии можно установить стент в просвет кишки. Хирургическое вмешательство следует проводить сразу же после диагностики непроходимости. Для лечения консервативные методы нецелесообразны, т. к. осложнение в виде прободения толстой кишки имеет чрезвычайно высокий коэффициент смертности.
Видео техники проведения очистительной клизмы
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Запор после операции
Соавтор, редактор и медицинский эксперт — Климович Элина Валерьевна.
Количество просмотров: 21 802
Дата последнего обновления: 25.08.2021 г.
Среднее время прочтения: 6 минут
Запор после операции не редкость в медицинской практике. Любое хирургическое вмешательство может повлиять на работу кишечника, причем даже если оно было проведено не на органах брюшной полости. Чтобы свести возможные неприятные последствия к минимуму, необходимо соблюдать рекомендации врача во время реабилитации.
Причины развития запора после операции
- Угнетающее влияние наркоза. В результате воздействия препаратов-миорелаксантов на организм человека все мышцы, в том числе и мышечный слой кишечной стенки, расслабляются, им требуется некоторое время, чтобы вновь прийти в тонус. Поэтому так часто в послеоперационном периоде возникают атонические запоры.
- Прием обезболивающих препаратов. Некоторые лекарственные средства, особенно опиоидные анальгетики, могут тормозить работу желудочно-кишечного тракта.
- Нарушение процессов пищеварения. Эта проблема возникает после операций на желудке, кишечнике, по удалению желчного пузыря и др. Организму требуется время для перестройки процессов пищеварения и нормализации выработки необходимых ферментов.
- Дисбактериоз. В период реабилитации для профилактики послеоперационных осложнений врачи часто назначают антибиотики. В качестве побочного эффекта от приема таких препаратов возможно нарушение баланса полезной микрофлоры кишечника.
- Длительное соблюдение постельного режима. Отсутствие двигательной активности на протяжении нескольких дней приводит к снижению тонуса мышц брюшного пресса, которые задействуются в том числе в продвижении каловых масс. Вследствие этого возникает запор.
- Изменение рациона. Послеоперационная диета также может быть причиной запора.
- Психологические причины. Многие пациенты после операции переживают из-за состояния швов или испытывают страх появления боли при натуживании (особенно если ранее был диагностирован геморрой), поэтому откладывают поход в туалет, чем провоцируют появление запора.
Симптомы запора
Невозможность акта дефекации на протяжении нескольких суток – основной признак запора. При этом пациент обычно чувствует тяжесть в животе. Его могут беспокоить тянущие боли. Нередко появляется метеоризм, поскольку газы также не отходят, а негативные процессы при застое каловых масс, наоборот, усиливаются. Постепенно развивается интоксикация организма. Пациента может мучить тошнота. У него ухудшается аппетит, нарушается сон, снижается настроение. Затвердевшие каловые массы могут травмировать слизистую и даже провоцировать небольшое кровотечение. Поэтому при акте дефекации в кале можно обнаружить слизь и кровь.
Общая схема лечения послеоперационных запоров
Иногда запор проходит сам, но в большинстве случаев он требует принятия тех или иных мер, особенно после операции, когда риск появления осложнений особенно велик. Если проблемы с дефекацией продолжаются несколько дней, при этом появляются другие неприятные симптомы, необходимо как можно скорее обратиться к врачу. Он поможет выявить причину и решить, что делать, чтобы устранить запор. Для борьбы с ним существует несколько методов. Многие из них можно комбинировать, чтобы добиться лучшего результата.
- Медикаментозная терапия. Назначить ее может только врач. При выборе препаратов обязательно учитывается тип проведенного хирургического вмешательства, состояние пациента и уже применяемые лекарственные средства.
- Соблюдение диеты и питьевого режима. Пациентам необходимо выпивать 1,5–2 л¹ жидкости в сутки. Если это вода, то она должна быть очищенной и без газа. Питание в послеоперационный период только дробное, небольшими порциями 5–6 раз в сутки. Диета зависит от вида операции. Но в любом случае нужно избегать продуктов, которые провоцируют газообразование (бобовые, капуста, редька, баклажаны) или оказывают вяжущее действие (груши, рис, манная каша, жирные бульоны из рыбы или мяса). При запоре лучше отдать предпочтение блюдам, содержащим клетчатку, натуральным сокам, кашам из цельных злаков, хлебу с отрубями и кисломолочным продуктам, если иную диету не назначил врач.
- Гимнастика или посильная физическая нагрузка. Каждый пациент после операции должен как можно быстрее начать двигаться (если нет противопоказаний). Длительный постельный режим провоцирует запоры. Если нельзя делать гимнастику, желательно хотя бы начать переворачиваться на постели и ходить пешком, постепенно увеличивая время прогулок. Комплекс упражнений обязательно необходимо согласовывать с врачом, поскольку при некоторых операциях такая физическая нагрузка противопоказана.
- Прием пре- и пробиотиков. Они необходимы для нормализации состава полезной микрофлоры в кишечнике.
- Аппаратный или мануальный массаж живота. Может назначаться врачом при отсутствии противопоказаний. Он выполняется в положении лежа, когда мышцы брюшного пресса максимально расслаблены. Один сеанс длится около 10 минут.
МИКРОЛАКС ® : помощь при запоре после операции
МИКРОЛАКС ® – это одноразовая микроклизма, которая содержит 5 мл препарата. Средство имеет высокий профиль безопасности и может применяться для борьбы с послеоперационными запорами. Активное вещество препарата МИКРОЛАКС ® способствует размягчению твердых каловых масс и их быстрому выведению. Микроклизма способствует наступлению действия через 5–15 минут¹ после применения.
Перед применением при послеоперационном запоре следует проконсультироваться с врачом.
Информация в данной статье носит справочный характер и не заменяет профессиональной консультации врача. Для постановки диагноза и назначения лечения обратитесь к квалифицированному специалисту.
Узнайте из нашего видео, чем вреден запор?
¹ Диетология. Руководство. Под редакцией А. Ю. Барановского. 4-е издание; Питер 2012.
Источник
Почему кишечник не работает после операции
Государственный научный центр колопроктологии им. А.Н. Рыжих Минздрава РФ, Москва
ФГБУ «ГНЦК им. А.Н. Рыжих» Минздрава России, Москва, Россия
Послеоперационный парез желудочно-кишечного тракта
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2017;(3): 76-85
Хомяков Е. А., Рыбаков Е. Г. Послеоперационный парез желудочно-кишечного тракта. Хирургия. Журнал им. Н.И. Пирогова. 2017;(3):76-85. https://doi.org/10.17116/hirurgia2017376-85
Государственный научный центр колопроктологии им. А.Н. Рыжих Минздрава РФ, Москва


Государственный научный центр колопроктологии им. А.Н. Рыжих Минздрава РФ, Москва
ФГБУ «ГНЦК им. А.Н. Рыжих» Минздрава России, Москва, Россия
В силу до конца не определенных факторов после операций на брюшной полости происходит нарушение нормальной согласованной пропульсивной моторики желудочно-кишечного тракта (ЖКТ). Это состояние динамической кишечной непроходимости называется послеоперационным парезом ЖКТ[25, 111, 121].
Клиническая картина послеоперационного пареза ЖКТ характеризуется невозможностью перорального приема пищи, отсутствием перистальтики, газов и стула на протяжении 5 дней после лапаротомии или в течение 3 дней после лапароскопической операции [44, 80, 109].
Актуальность проблемы
Парез ЖКТ — одно из наиболее часто встречающихся послеоперационных осложнений [1, 11, 90].
Члены ассоциации колопроктологов Великобритании и Ирландии поставили парез ЖКТ на 5-е место в списке актуальных проблем колопроктологии [119].
Пациенты с кишечной непроходимостью обездвижены, испытывают дискомфорт и боль, у них возрастает риск легочных осложнений. Паралитическая кишечная непроходимость — важная причина длительной госпитализации [43, 80].
Об актуальности проблемы также свидетельствует тот факт, что расходы на лечение пациентов при развитии такого осложнения возрастают значительно. Так, S. Iyer и соавт. [63] ретроспективно оценили затраты на лечение пациентов с парезом ЖКТ в послеоперационном периоде, проанализировав 17 876 наблюдений. Средняя продолжительность госпитализации пациентов с послеоперационным парезом ЖКТ (13,8 дня) была значимо больше, чем пациентов без пареза (8,9 дня) (p 
Обзорная рентгенограмма органов брюшной полости — первое диагностическое звено при жалобах пациента на вздутие живота, тошноту или боль. Обзорный снимок делается в положении больного на спине и в вертикальном положении. При парезе ЖКТ визуализируются расширенные за счет газа петли кишечника без зоны переходов (которые предполагают механическую непроходимость кишечника) и без скоплений газа в свободной брюшной полости (наблюдается при перфорации полых органов) [63]. Рентгенологические исследования с контрастным усилением (пассаж бария или ирригоскопия) также играют важную роль в дифференциальной диагностике послеоперационного пареза ЖКТ и механической кишечной обструкции [2].
Если диагноз неясен, возможно проведение компьютерной томографии органов брюшной полости [63, 64]. КТ брюшной полости имеет чувствительность 90%, а специфичность 100% в дифференциальной диагностике механической кишечной непроходимости [63]. Кроме того, КТ брюшной полости нередко может выявить вторичные причины пареза или непроходимости, например абсцессы малого таза, гематомы, а в случае механической непроходимости — локализовать место обструкции [118].
Лабораторная оценка направлена на выявление обратимых факторов, которые могут способствовать послеоперационному парезу ЖКТ, или на поиск другого послеоперационного осложнения. В лабораторных исследованиях имеются метаболические и электролитные изменения в крови. В исследование U. Kronberg и соавт. [74] были включены 413 пациентов, перенесших лапароскопическую резекцию толстой кишки, у 42 из которых имел место послеоперационный парез ЖКТ. Согласно полученным результатам, сывороточный уровень кальция был достоверно ниже у пациентов с парезом (8,14 ммоль/л против 8,29 ммоль/л; p=0,042; ОШ=0,69); медиана концентрации магния в послеоперационном периоде была несколько выше в группе пациентов с парезом (1,92 ммоль/л против 1,82 ммоль/л; p=0,09). При анализе медианы послеоперационной концентрации калия в плазме крови достоверных различий между группами получено не было (3,97 ммоль/л против 3,94 ммоль/л; p=0,55). Тем не менее при сравнении минимальных показателей концентрации калия самый низкий показатель отмечался в группе пациентов с парезом ЖКТ (3,43 ммоль/л против 3,66 ммоль/л; p 2 -индекс=63,34%), исследование E. Orlando и соавт. [98] было удалено из анализа; эффективность неостигмина в лечении пареза ЖКТ составила 95,6% по сравнению с 0,00 в контрольной группе. Важно отметить, что включение в метаанализ только четырех исследований с однозначными выводами подразумевает слишком низкую силу анализа для реальной оценки эффективности препарата [123].
Метаанализ эффективности фармакологического лечения пареза ЖКТ, проведенный U. Traut и соавт. [122], включал 39 рандомизированных контролируемых исследований и показал, что использование большинства имеющихся в арсенале клинициста препаратов (в том числе эритромицина, холецистокинина, цизаприда и антагонистов допамина) не оправдано. Авторы также пришли к выводу, что неостигмин усиливает перистальтику кишечника, однако необходимы дополнительные исследования, посвященные безопасности и эффективности препарата в лечении послеоперационного пареза ЖКТ.
Большая часть исследований, посвященных использованию неостигмина в лечении пареза ЖКТ, отличается малой выборкой пациентов с несопоставимыми контрольными группами, в них использованы различные дозы и пути введения неостигмина, они не имеют радиологического подтверждения разрешения [14, 15]. Таким образом, необходимы крупные рандомизированные исследования с большой выборкой пациентов для лучшего понимания и интерпретации полученных результатов [68].
Поскольку воспаление может также привести к развитию послеоперационного пареза ЖКТ (абсцесс в брюшной полости или в полости малого таза, сепсис или раневая инфекция, хирургическая травма кишечника), меры, направленные на его предупреждение, могут быть эффективны в периоперационном периоде [23]. Данные отдельных клинических испытаний, посвященных изучению роли только нестероидных противовоспалительных препаратов в профилактике пареза ЖКТ, отсутствуют, но их использование как компонента медикаментозного сопровождения послеоперационного периода оправдано, по мнению C. Delaney [44] и J. Grass и соавт. [56].
Учитывая отрицательное воздействие опиоидов на моторику ЖКТ, ингибирование активации μ-опиоидных рецепторов — оптимальная мишень опиоидно-индуцированной дисфункции кишечника. В данном контексте проходят клинические испытания два препарата — альвимопан и метилналтрексон [45, 125].
Альвимопан и метилналтрексон — периферические антагонисты μ-опиоидных рецепторов, прошли клинические испытания и, как было показано, значительно сократили по сравнению с плацебо сроки восстановления перистальтики (18—22 ч) после оперативного вмешательства на брюшной полости и полости малого таза [45].
Альтернативные методы лечения послеоперационного пареза ЖКТ, например прием слабительных препаратов, мало изучены. В одном рандомизированном исследовании пациенты получали бисакодил или плацебо 2 раза в день, начиная с первого дня после операции. В группе получавших бисакодил отмечалось сокращение сроков отхождения первого стула по сравнению с группой плацебо — 25 ч и 56 ч соответственно. Тем не менее необходимы дальнейшие исследования для оценки действия слабительных препаратов на послеоперационный парез ЖКТ [60].
Определенный интерес также представляет электростимуляция ЖКТ [79], однако сведения об эффективности этого метода недостаточны [35].
Профилактика
Практический опыт лечения послеоперационного пареза свидетельствует о том, что борьба с ним начинается лишь тогда, когда он уже развивается, в то время как мероприятия по лечению пареза должны проводиться в раннем послеоперационном периоде до появления его клинических признаков [1—3, 5].
Предупреждение послеоперационного пареза ЖКТ — эффективная стратегия с позиций сокращения сроков пребывания пациентов в стационаре, с экономических позиций и с точки зрения самого пациента. Имеющиеся данные литературы позволяют выделить несколько потенциально эффективных стратегий снижения клинических последствий послеоперационной динамической кишечной непроходимости, в том числе минимизацию интраоперационной травмы, использование эпидуральной анестезии с расположением катетера в среднегрудном отделе, что сводит к минимуму потребность в опиоидных анальгетиках для снижения выраженности болевого синдрома[43].
H. Jorgensen и соавт. [64] в кокрановском систематическом обзоре 22 литературных источников сравнили действие эпидуральной анестезии и опиоидных анальгетиков на развитие послеоперационного пареза ЖКТ, появление тошноты и рвоты, а также увеличение выраженности болевого синдрома после операции на брюшной полости. Согласно полученным результатам, использование эпидуральных местных анестетиков позволило сократить сроки восстановления кишечной функции — 24 ч против 37 ч при использовании системных опиоидных анальгетиков (оценивалось время отхождения газов или первого стула). Авторы также обнаружили, что добавление центральных (опиоидных) анальгетиков к местным при эпидуральной анестезии обеспечивает более выраженный обезболивающий эффект по сравнению с применением только местных анальгетиков без увеличения вероятности развития пареза ЖКТ. Тем не менее J. Neudecker и соавт. [95], R. Kuruba и соавт. [75] не смогли воспроизвести результаты предыдущих исследований, оценивающих влияние эпидуральной анестезии на продолжительность послеоперационного пареза после лапароскопической резекции ободочной кишки.
Было доказано, что лапароскопическая хирургия (в том числе при колоректальном раке) и применение малоинвазивных методов лечения способствуют уменьшению болей в послеоперационном периоде, потребности в анальгетиках, более быстрому восстановлению дыхательной функции и, как следствие, меньшей продолжительности пребывания пациента в стационаре [99, 104]. Согласно проведенным рандомизированным исследо
Источник